第3回 燃料電池に使われる『膜』(作動メカニズムと技術課題)
燃料電池自動車が走り始め、実用でのデータの分析はできるようになったが、この先の開発進展に向けて、心臓部である
発電膜『セル』の基礎的な性能や原理の解析、シミュレーション技術が強く求められるようになった。
今回は、燃料電池のセルの中で分子レベルでの反応メカニズムと物質の移動により、どのように性能が実現されるのかに
そって、その実力と課題について述べる。
1.セル反応部分の構造
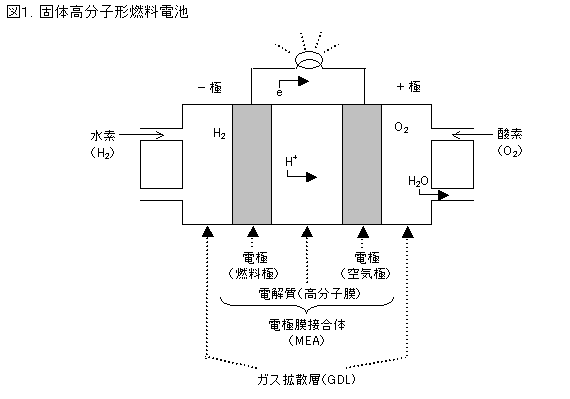
2.ガス拡散層(GDL)
ガス拡散層は電極上の触媒に、反応ガス(水素、酸素)を管理しながら供給する機能を担っている。カーボン繊維で
ペーパー状につくる。ガスの主な移動メカニズムは、濃度拡散であるが、分子運動速度の速い水素側に比べて、水の発生
する空気極側はかなり難しい。特に出力が変動すると発生する水の量も変動する。排水性をよくすると、局部的に電極が
乾燥して具合が悪い。保湿側にすると、結露水がつまって、空気が電極にとどかなくなる。この設計によって、拡散分極
での出力密度が律速される。微細形態の改良や親水性、撥水性の非均質加工、ガス加湿など細かな工夫により、
実用運転範囲での排水性を確保するが、膜面積が大きくなると、部分乾燥と部分結露がさけられない。現状は結露側で使用
する時、水拡散が間に合わず分極がおき、出力限界となっている。
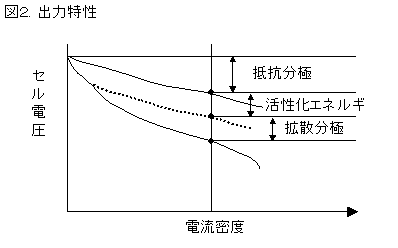
3.電極膜接合体(MEA)
電極膜接合体は、イオン交換機能を持つ樹脂でできた電解質膜を電極ではさんで作る。ただはさんだだけでは電解質が
電極に触れる部分が少なく、イオンがうまく流れず、電極の触媒が有効に働いてくれない。接合部の電極に電解質の粉を混ぜるなどして、一体化成型される。
3-1.燃料極
電気を伝えるカーボン粒を固めて構成され、カーボンの表面に白金微細粒子をまぶしてある。白金表面に水素分子が
ぶつかり吸着されると、運動の自由度が減るため、分子が解体される。さらに表面に沿って加速され、電解質界面にてイオン化した状態で白金表面を離脱するものも出てくる。電極間の電位により、この水素イオンは空気極に向かって電解質中を
移動し、電流源となる。イオン化したとき放出される自由電子は、カーボン電極を通って電気負荷を流れる。
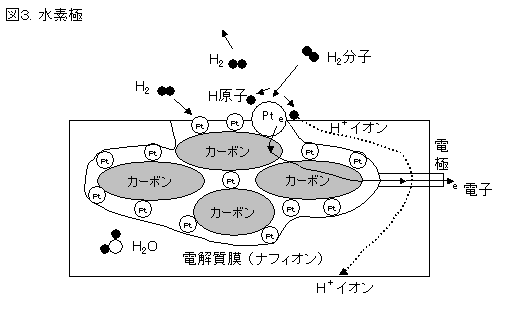
触媒作用をするのが白金表面であるので、表面積をおおきくするため、微細な粉末白金『白金黒』を用いる。さらに粒子を
細かくして白金使用量を10分の1ほどにするのが課題である。現状はFCV1台あたり100g以上もの白金が使われている。
勿論微細化に伴い、表面エネルギの高い状態を保つことになるので、カーボン上電解質中での安定性(離脱、粒子結合
砂金化)、などの課題も大きくなる。
3-2.空気極
燃料極と同じ白金電極構造が一般的である。空気極では、電解質を通じて運ばれた水素イオンと白金表面に吸着された
酸素が反応して水が生成される。水素イオンは電子をもらうので、水素と酸素の反応が電気エネルギに変換される。
燃料極と大きく異なるのは、白金表面に大量の水が存在することである。吸着された酸素は、白金表面で水素イオンと
順次結合し、まずHOOHの形になる。つぎに、0.5eV 程度のポテンシャル障壁を越えて水となる。
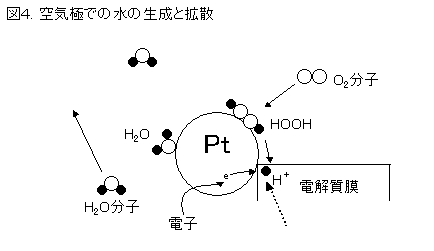
水は白金表面を離脱するためには、さらに0.5eV程度のポテンシャルが必要であり、表面をおおう水の除去が反応速度に
大きく影響する。またHOOHが水になるときの条件によって、活性酸素が発生すると、電解質膜の炭素結合をアタックし、
劣化故障の原因になる。したがって、活性酸素の発生を抑えながら水離脱を促進する触媒反応設計が求められるが、
運転温度と出力が短時間に変動すると反応制御は難しい。
3-3.電解質膜
現在はパーフルオロ系のイオン交換樹脂(ナフィオン)が主流である。耐熱性が80度Cと低く、信頼性耐久性も今ひとつで
ある。コスト的にも10万円/m2 とまだ高い。
膜の要求機能はガスシール性、イオン伝達性、電極絶縁性などである。
ガスシールは水素が膜を透過して直接空気極側に行くと、触媒上で酸素と結合するが、電気的な作用が無いので、発電
せず燃料としては無駄になる。水素分子は透過性が強いので、静的なシールは困難であり、水素極でなるべく多く反応
するようなMEAとしての構造設計が求められる。
膜の厚さは薄いほうが反応上は高性能になるが、穴明きなど強度上の限界がある。補強ネットを追加して強度機能を分担
させる研究もおこなわれている。
イオン交換樹脂らしい膜の機能は、水素イオン伝達のメカニズムである。
イオン伝達メカニズムを担う要素は水とスルホ基で、伝達の原動力は電場と分子運動である。
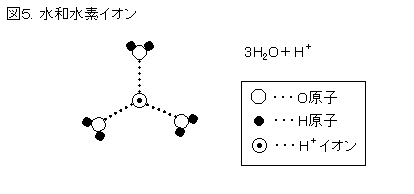
まず水素極で分離した水素イオンは、水和して、H+ 3(H2O) (図5)などの形になって、プラスの電荷をもつかたまりで、電場に
より空気極に引き寄せられてゆく。送金にたとえると現金書留のようなやり方で、ビーグルと呼ばれる。
もうひとつの移動は銀行振込のようなグロータスと呼ばれる移動で、これは2種類ある。
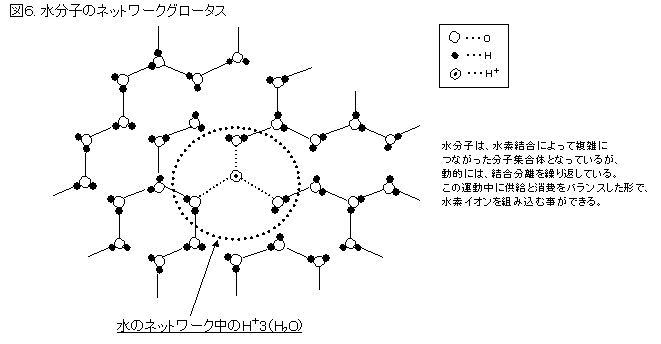
ひとつは水の分子ネットワーク中にH+が入り、分子運動によるネットワーク構造の変化によって、H+が拡散して、空気極で
消費されるH+と統計的に相殺されるネットワークグロータスである。
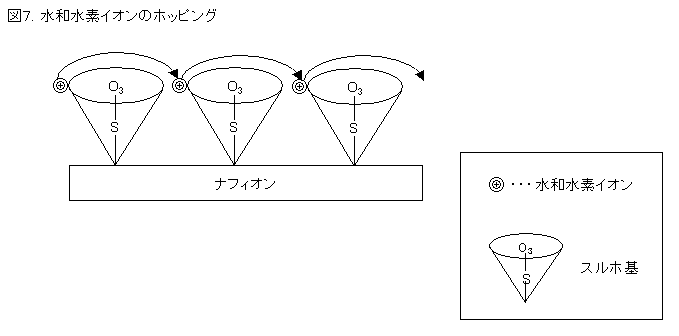
もうひとつは、ナフィオンの端にあるスルホ基の酸素部分の回転運動を介して水和イオンが飛び石状に受け渡される、
ホッピングと呼ばれる移動である。
しかし見て来たように言うものの、運動状態の分子では計測も難しく、どのくらいの割合でこれらのメカニズムがイオン伝導に寄与しているのかは、よくわかっていない。
というわけで、燃料電池の基本性能は、分子レベルでの材料設計や、温度湿度圧力ごとの反応制御などによって、大きな
影響を受ける。性能向上や耐久性の確保といった課題の解決には、計測技術やシミュレーション手法など、材料を分子運動
レベルで解析し設計するための先導的な基礎技術研究が、今おおきな役割を担っている。
|